Советы агронома
По размеру сад должен быть таким,чтобы за ним могла ухаживать твоя жена. Томас Эверетт
Кислотность почвы
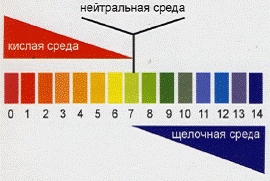
Само понятие кислотности почвы относится к реакции среды, которая может быть как кислой, так и щелочной (противоположность кислотной). Зависит реакция среды от соотношения в почвенном растворе ионов H+ и OH-. В состав неорганических кислот входит водород, отсюда, чем выше концентрация ионов водорода H+, тем почва кислее, чем меньше – тем она более щелочная. Обозначается реакция среды как pH (пэ аш).
Реакция среды pH - это сокращение от pondus Hydrogenii (лат.), что буквально на русский язык переводится как "сила водорода". То есть так обозначается мера активности ионов водорода и количественно выражается кислотность среды. Понятие pH было введено в 1909 году датским химиком Сёреном Сёренсеном.
Нейтральная реакция почвы соответствует рН 7. Если рН выше 7, то реакция почвы щелочная, ниже — кислая. При этом кислые почвы классифицируются следующим образом:
- очень кислые — рН находится в пределах 3,8-4,0;
- сильнокислые — рН 4,1-4,5;
- среднекислые — рН 4,6-5,0;
- слабокислые — рН 5,1-5,5;
- близкие к нейтральной — рН 5,6-6,9.
На кислотность почв (pH) может влиять множество факторов. Их условно можно разделить на естественные (природные) и антропогенные (т.е. деятельность человека). Так наиболее кислую реакцию имеют верховые болотные почвы, но их кислотность может смещаться под воздействием человеческой деятельности: при перемещении пластов почвы при строительстве или при выравнивании участка, сильно подкисляют почву многие минеральные удобрения (аммиачная селитра, хлористый калий и др.).
Растения поглощают через корни только те питательные элементы (азот, фосфор, железо и др.), которые за счет химических реакций находятся в почве в виде ионов (т.е. в растворенном состоянии). Если не вдаваться в детали, то реакция среды влияет на то, как и какие элементы питания растворяются в почве, а, значит, и на их доступность для растений.
В учебниках агрохимии указывается, что в кислой среде усиливается растворение малорастворимых солей, при этом увеличивается содержание доступных форм железа, марганца, кобальта, меди, алюминия, они накапливаются в почве, что приводит к отравлению растений высокими концентрациями этих элементов, – накапливаясь в растениях, они препятствуют поступлению других, более полезных.
Несмотря на отрицательное действие кислых почв, большинство растений хорошо растет и развивается при слабокислой реакции среды (pH 5,5-6,5), так как в этих условиях увеличивается количество доступных полезных элементов питания, при этом не накапливается значительное количество вредных (алюминий). Например, для томата оптимальная кислотность – pH 5,5-5,8, а для огурца – pH 6,2-6,2. А вот при pH 4-5 рост огурца уже подавляется.
Значительное снижение кислотности и повышение щелочности (pH > 7) приводит к тому, что фосфор, кальций, марганец, железо, цинк и бор выпадают в осадок в форме фосфорнокислых и углекислых солей, малодоступных для растений. Опять же растения страдают от недостатка нужных им элементов и их рост угнетается.
Для нейтрализации кислотности рекомендуют вносить золу или известь. Из вышесказанного становится понятно, что стоит переборщить с их количеством и эффект будет противоположным. А точнее таким же, как и до известкования – растения недополучат питание из-за высокой щелочности почв. Поэтому правило «чем больше, тем лучше» в данном случае не действует.
Большинство овощных культур предпочитает почву, близкую к нейтральной. К таким растениям относятся морковь, свекла, сельдерей, лук, чеснок, почти все виды капусты, клевер. Для них оптимальное значение рН составляет 6-7.
На слабокислых почвах хорошо произрастают огурцы, тыква, редис, редька, томаты, кабачки, горох, ревень.
Более устойчивы к повышенной кислотности люпин, картофель.
На почвах с высокой кислотностью — щавель.
Из плодовых и ягодных культур при рН почв 5-7 хорошо растут и плодоносят яблоня, груша, слива, вишня, облепиха, черная смородина, крыжовник, земляника.
Ленинградская область, Всеволожский район, Лесколовская волость, район деревни Верхние Осельки, ж/с Пери
Плагиат не преследуется!